Autor:
Monica Porter
Dátum Stvorenia:
17 Pochod 2021
Dátum Aktualizácie:
1 V Júli 2024

Obsah
Molárna koncentrácia označuje vzťah medzi počtom mólov rozpustenej látky a objemom roztoku. Ak chcete vypočítať molaritu, môžete začať s molami a objemom, hmotnosťou a objemom alebo molami a mililitrami (ml). Potom s premennými vyššie použite základný vzorec molárnej koncentrácie, aby ste dosiahli správny výsledok.
Kroky
Metóda 1 zo 4: Výpočet molárnej koncentrácie z molárneho čísla a objemu
Je dôležité poznať základný vzorec pre výpočet molárnej koncentrácie. Molárna koncentrácia rovná počtu mólov rozpustenej látky vydelená objemom roztoku v litroch. Odtiaľ máme nasledujúci vzorec: Molárna koncentrácia = počet mólov rozpustenej látky / počet litrov roztoku
- Príklad: Aká je molárna koncentrácia roztoku obsahujúceho 0,75 mol NaCl v 4,2 litroch roztoku?

Analyzuj tému. Na výpočet molárnej koncentrácie potrebujete počet mólov a objem roztoku v litroch. Tieto dve hodnoty nemusíte počítať kvôli danej téme.- Napríklad:
- Počet mólov = 0,75 mólu NaCl
- Objem = 4,2 l
- Napríklad:
Počet mólov vydelte objemom. Výsledkom rozdelenia mólov na objem je počet mólov na liter roztoku alebo molárna koncentrácia tohto roztoku.
- Príklad: molárna koncentrácia = počet mólov rozpustenej látky / počet litrov roztoku = 0,75 mol / 4,2 l = 0,17857142

Zaznamenajte si svoje výsledky. Zaokrúhlite na dve alebo tri čísla za čiarkou, v závislosti od požiadavky učiteľa alebo zadania. Pri zaznamenávaní výsledkov skráťte výraz „molárna koncentrácia“ na „M“ a zahrňte chemický symbol rozpustenej látky.- Napríklad: 0,179 M NaCI
Metóda 2 zo 4: Vypočítajte molárnu koncentráciu z objemu a objemu
Je potrebné poznať základný vzorec pre výpočet molárnej koncentrácie. Molárna koncentrácia ukazuje vzťah medzi počtom mólov rozpustenej látky a objemom roztoku. Vzorec pre molárnu koncentráciu je nasledovný: molárna koncentrácia = koncentrácia rozpustenej látky / počet litrov roztoku
- Príklad problému: Vypočítajte počet mólov roztoku po rozpustení 3,4 g KMnO4 v 5,2 litroch vody.

Analyzuj tému: Na zistenie molárnej koncentrácie potrebujete počet mólov a objem roztoku v litroch. Ak tieto hodnoty nie sú uvedené, ale poznáte objem a hmotnosť roztoku, môžete pred výpočtom molárnej koncentrácie určiť počet mólov rozpustenej látky.- Napríklad:
- Hmotnosť = 3,4 g KMnO4
- Objem = 5,2 l
- Napríklad:
Vypočítajte hmotnostnú molekulu rozpustenej látky. Ak chcete vypočítať počet mólov rozpustenej látky z tejto hmotnosti alebo gramov rozpustenej látky, musíte najskôr určiť hmotnostnú molekulu rozpustenej látky. Hmotnostnú molekulu rozpustenej látky je možné určiť pridaním hmotnostného atómu každého prvku v roztoku. Na nájdenie kubického atómu každého prvku použite periodickú tabuľku prvkov.
- Napríklad:
- Hmotnostný atóm K = 39,1 g
- Hmotnostný atóm Mn = 54,9 g
- Hmotnostný atóm O = 16,0 g
- Celkové atómy hmotnosti = K + Mn + O + O + O + O = 39,1 + 54,9 + 16 + 16 + 16 + 16 = 158,0 g
- Napríklad:
Preveďte gramy na krtky. Keď máte kubickú molekulu, musíte vynásobiť počet gramov rozpustenej látky v roztoku ekvivalentným konverzným faktorom 1 mol na molárnu hmotnosť rozpustenej látky. Výsledkom tohto násobenia je počet mólov rozpustenej látky.
- Príklad: gramy rozpustenej látky * (1 / molárna hmotnosť rozpustenej látky) = 3,4 g * (1 mol / 158 g) = 0,0215 mol
Počet mólov vydelte počtom litrov. Teraz, keď ste vypočítali počet mólov, teraz toto číslo vydelte objemom roztoku v litroch, budete mať molárnu koncentráciu tohto roztoku.
- Príklad: molárna koncentrácia = počet mólov rozpustenej látky / počet litrov roztoku = 0,0215 mol / 5,2 l = 0,004134615
Zaznamenajte si svoje výsledky. Výsledky musíte zaokrúhliť podľa požiadaviek učiteľa, zvyčajne dve až tri čísla za čiarkou. Okrem toho pri písaní výsledku skráťte výraz „molárna koncentrácia“ ako „M“ a sprevádzajte chemický symbol rozpustenej látky.
- Napríklad: 0,004 M KMnO4
Metóda 3 zo 4: Vypočítajte molárnu koncentráciu z počtu mólov a mililitrov roztoku
Potrebujete poznať vzorec pre molárnu koncentráciu. Na výpočet molárnej koncentrácie. Musíte vypočítať počet mólov rozpustenej látky na liter roztoku, nie mililiter roztoku. Všeobecný vzorec pre výpočet molárnej koncentrácie je: molárna koncentrácia = počet mólov rozpustenej látky / počet litrov roztoku
- Príklad: Vypočítajte molárnu koncentráciu roztoku obsahujúceho 1,2 mólu CaCl2 v 2905 mililitroch vody.
Analyzuj tému. Na výpočet molárnej koncentrácie potrebujete počet mólov rozpustenej látky a objem roztoku v litroch. Ak je objem roztoku uvedený v úlohe v mililitroch, pred výpočtom prepočítajte na ekvivalentný objem v litroch.
- Napríklad:
- Počet mólov = 1,2 mólu CaCl2
- Objem = 2905 ml
- Napríklad:
Preveďte mililitre na liter. Ak chcete previesť roztok z mililitrov na liter, počet mililitrov vydelte 1000, pretože každý liter sa rovná 1000 mililitrom. Mililitre môžete tiež previesť na liter posunutím desatinnej čiarky o 3 číslice doľava.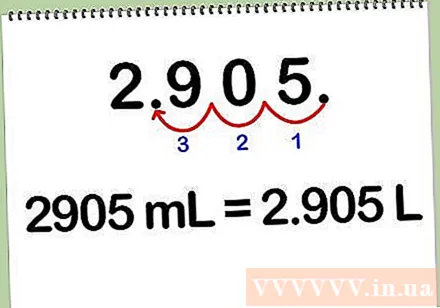
- Napríklad: 2905 ml * (1 l / 1000 ml) = 2 905 l
Počet mólov vydelte počtom litrov. Po získaní počtu litrov môžete vypočítať molárnu koncentráciu vydelením počtu mólov počtom litrov roztoku.
- Príklad: molárna koncentrácia = počet mólov rozpustenej látky / počet litrov roztoku = 1,2 mólu CaCl2 / 2 905 L = 0,413080895
Zaznamenajte si svoje výsledky. Výsledok nezabudnite zaokrúhliť na dve alebo tri čiarky alebo na žiadosť učiteľa. Pri zaznamenávaní výsledkov použite skratku „molárna koncentrácia“ ako „M“ a potom chemický symbol pre rozpustenú látku.
- Napríklad: 0,413 M CaCl2
Metóda 4 zo 4: Extra prax
Vypočítajte molárnu koncentráciu roztoku, keď sa 5,2 g NaCl rozpustí v 800 ml vody. Určte hodnoty dané problémom: hmotnosť v gramoch a objem v mililitroch.
- Hmotnosť = 5,2 g NaCI
- Objem = 800 ml vody
Nájdite masovú molekulu NaCl pridaním kubického atómu prvku Na a kubického atómu Cl.
- Hmotnostný atóm Na = 22,99 g
- Hmotnostný atóm Cl = 35,45 g
- Hmotnostné molekuly NaCl = 22,99 + 35,45 = 58,44 g
Vynásobte hmotnosť rozpustenej látky molárnym konverzným faktorom. V tomto príklade je molekulová hmotnosť NaCl 58,44 g, takže konverzný faktor je „1 mol / 58,44 g“.
- Počet mol NaCl = 5,2 g NaCl * (1 mol / 58,44 g) = 0,8898 mol = 0,09 mol
Rozdeľte 800 ml vody na 1000, získate objem vody v litroch.
- 800 ml môžete tiež vynásobiť konverzným faktorom 1 l / 1000 ml z mililitra na liter.
- Ak chcete skrátiť postup násobenia, ako je uvedené vyššie, môžete desatinnú čiarku posunúť späť o 3 číslice doľava.
- Objem = 800 ml * (1 l / 1 000 ml) = 800 ml / 1 000 ml = 0,8 l
Počet mólov rozpustenej látky vydelte objemom roztoku v litroch. Ak chcete vypočítať molárnu koncentráciu, musíte vydeliť 0,09 molu rozpustenej látky (v tomto prípade NaCl) objemom roztoku v litroch.
- Molárna koncentrácia = počet mólov rozpustenej látky / počet litrov roztoku = 0,09 mol / 0,8 l = 0,1125 mol / l
Zaznamenajte konečný výsledok. Výsledok zaokrúhlite na dve alebo tri čísla za čiarkou a skratku „molárna koncentrácia“ označte „M“ spolu s chemickým symbolom rozpustenej látky.
- Výsledok: 0,11 M NaCI