Autor:
Judy Howell
Dátum Stvorenia:
27 V Júli 2021
Dátum Aktualizácie:
23 V Júni 2024

Obsah
- Na krok
- Časť 1 zo 4: Pochopenie štruktúry
- Časť 2 zo 4: Pochopenie symbolu a pomenovania
- Časť 3 zo 4: Čítanie atómového čísla
- Časť 4 zo 4: Odčítanie atómovej hmotnosti
Periodická tabuľka prvkov je zoznamom doteraz objavených 118 prvkov. Existuje niekoľko symbolov a čísel, ktoré označujú rozdiely v prvkoch, zatiaľ čo štruktúra tabuľky organizuje prvky podľa podobností. Periodickú tabuľku si môžete prečítať podľa pokynov uvedených nižšie.
Na krok
Časť 1 zo 4: Pochopenie štruktúry
 Myslite na to, že periodická tabuľka začína v ľavom hornom rohu a končí na konci posledného riadku v dolnej a pravej časti. Tabuľka je štruktúrovaná zľava doprava v poradí stúpajúceho atómového čísla. Atómové číslo je počet protónov v jednom atóme.
Myslite na to, že periodická tabuľka začína v ľavom hornom rohu a končí na konci posledného riadku v dolnej a pravej časti. Tabuľka je štruktúrovaná zľava doprava v poradí stúpajúceho atómového čísla. Atómové číslo je počet protónov v jednom atóme. - Nie každý riadok alebo stĺpec je úplný. Aj keď môžu byť v strede medzery, čítajte tabuľku zľava doprava. Napríklad vodík má atómové číslo 1 a je umiestnený v ľavom hornom rohu. Hélium má atómové číslo 2 a je v pravom hornom rohu.
- Prvky 57 až 71 sú zvyčajne zobrazené ako podmnožina v pravom dolnom rohu tabuľky. Toto sú „prvky vzácnych zemín“.
 V každom stĺpci tabuľky nájdete „skupinu“ prvkov. Je tu 18 stĺpcov.
V každom stĺpci tabuľky nájdete „skupinu“ prvkov. Je tu 18 stĺpcov. - Na čítanie zhora nadol používajte výraz „čítanie skupiny“.
- Číslovanie je zvyčajne uvedené nad stĺpcami; môže to však byť aj pod inými skupinami, ako sú napríklad kovy.
- Číslovanie použité v periodickej tabuľke sa veľmi líši. Môžu to byť rímske (IA), arabské (1A) alebo číslice 1 až 18.
- Vodík môže byť v skupine halogénov a v alkalických kovoch alebo v obidvoch.
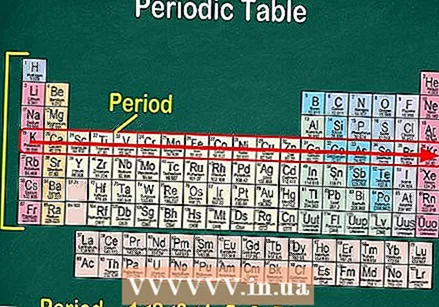 V každom riadku tabuľky nájdete „bodky“ prvkov. K dispozícii je 7 období. Pomocou výrazu „čítať po bodke“ čítajte zľava doprava.
V každom riadku tabuľky nájdete „bodky“ prvkov. K dispozícii je 7 období. Pomocou výrazu „čítať po bodke“ čítajte zľava doprava. - Obdobia sú zvyčajne očíslované od 1 do 7 na ľavej strane tabuľky.
- Každé obdobie je väčšie ako posledné. Súvisí to so zvyšovaním energetických hladín atómov v periodickej tabuľke.
 Pochopte ďalšie skupiny týkajúce sa kovových, polokovových a nekovových. Farby sa veľmi líšia.
Pochopte ďalšie skupiny týkajúce sa kovových, polokovových a nekovových. Farby sa veľmi líšia. - Skupina Kovy má jednu farbu. Vodík má však často rovnakú farbu a skupinu ako nekovy. Kovy majú lesk, zvyčajne sú pri izbovej teplote tuhé, vedú teplo a elektrinu a sú tvárne a tvárne.
- Rovnakú farbu majú aj nekovy. Sú to prvky C-6 až Rn-86, vrátane H-1 (vodík). Nemajú lesk, vedú teplo a elektrinu a nie sú tvárne. Spravidla tvoria plyn pri izbovej teplote a môžu to byť tuhé látky, plyny alebo kvapaliny.
- Polokovy / metaloidy majú zvyčajne fialovú alebo zelenú farbu ako kombináciu ďalších dvoch farieb. Čiara je diagonálna a siaha od prvkov B-5 po At-85. Majú niektoré vlastnosti kovov a niektoré nekovov.
 Upozorňujeme, že prvky sú niekedy uvedené aj v rodinách. Jedná sa o alkalické kovy (1A), kovy alkalických zemín (2A), halogény (7A), vzácne plyny (8A) a atómy uhlíka (4A).
Upozorňujeme, že prvky sú niekedy uvedené aj v rodinách. Jedná sa o alkalické kovy (1A), kovy alkalických zemín (2A), halogény (7A), vzácne plyny (8A) a atómy uhlíka (4A). - Číslovanie môže byť rímske, arabské alebo štandardné čísla.
Časť 2 zo 4: Pochopenie symbolu a pomenovania
 Najskôr si prečítajte symbol. Skladá sa z jedného alebo dvoch písmen a je štandardný vo viacerých jazykoch.
Najskôr si prečítajte symbol. Skladá sa z jedného alebo dvoch písmen a je štandardný vo viacerých jazykoch. - Symbol môže byť odvodený z latinského názvu prvku alebo jeho bežnej bežnej nominálnej hodnoty.
- V mnohých prípadoch sa symbol riadi anglickou konvenciou pomenovania, napríklad Hélium alebo „He“. Nie je to však pravidlo, ktoré môžete predpokladať. Napríklad železo je „Fe“. Z tohto dôvodu je kombinácia znakov a mien zvyčajne zapamätaná pre rýchlu orientáciu.
 Pozrite sa na bežný názov. Toto je priamo pod symbolom. To sa líši v závislosti od jazyka, v ktorom je periodická tabuľka napísaná.
Pozrite sa na bežný názov. Toto je priamo pod symbolom. To sa líši v závislosti od jazyka, v ktorom je periodická tabuľka napísaná.
Časť 3 zo 4: Čítanie atómového čísla
 Periodickú tabuľku čítajte podľa atómového čísla v strede hornej časti poľa každého prvku. Ako už bolo spomenuté, systém je radený zhora zľava doprava dole. Poznanie atómového čísla je najrýchlejší spôsob, ako vyhľadať viac informácií o prvku.
Periodickú tabuľku čítajte podľa atómového čísla v strede hornej časti poľa každého prvku. Ako už bolo spomenuté, systém je radený zhora zľava doprava dole. Poznanie atómového čísla je najrýchlejší spôsob, ako vyhľadať viac informácií o prvku. 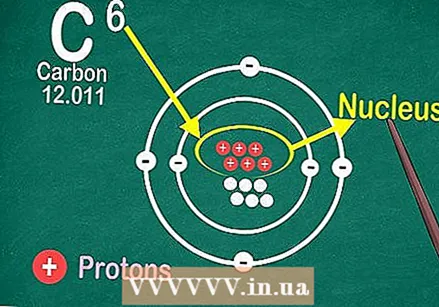 Atómové číslo je počet protónov v jadre jedného atómu prvku.
Atómové číslo je počet protónov v jadre jedného atómu prvku. Pridaním alebo odstránením protónov sa vytvorí iný prvok.
Pridaním alebo odstránením protónov sa vytvorí iný prvok. Zistenie počtu protónov v atóme určuje aj počet elektrónov. Atómy majú toľko elektrónov ako protóny.
Zistenie počtu protónov v atóme určuje aj počet elektrónov. Atómy majú toľko elektrónov ako protóny. - Pamätajte, že z tohto pravidla existuje výnimka. Keď atóm stratí alebo získa elektróny, stane sa z neho elektricky nabitý ión.
- Ak je vedľa symbolu prvku znamienko plus, znamená to, že je kladne nabitý. So symbolom mínus je negatívne nabitý.
- Ak nie je žiadny symbol plus alebo mínus a váš chemický problém sa netýka iónov, potom je počet protónov a elektrónov pravdepodobne rovnaký.
Časť 4 zo 4: Odčítanie atómovej hmotnosti
 Určte atómovú hmotnosť. Toto je číslo pod bežným názvom prvku.
Určte atómovú hmotnosť. Toto je číslo pod bežným názvom prvku. - Aj keď sa môže zdať, že atómová hmotnosť rastie z ľavého horného rohu systému dole vpravo, nie je to pravda vo všetkých prípadoch.
 Pochopte, že väčšinu prvkov predstavujú desatinné miesta. Atómová hmotnosť je súčet častíc v jadre; je to však vážený priemer rôznych izotopov.
Pochopte, že väčšinu prvkov predstavujú desatinné miesta. Atómová hmotnosť je súčet častíc v jadre; je to však vážený priemer rôznych izotopov.  Pomocou atómovej hmotnosti nájdite počet neutrónov v jednom atóme. Atómovú hmotnosť zaokrúhlite na najbližšie celé číslo, číslo hmotnosti. Potom odčítate počet protónov od hromadného čísla, aby ste určili počet neutrónov.
Pomocou atómovej hmotnosti nájdite počet neutrónov v jednom atóme. Atómovú hmotnosť zaokrúhlite na najbližšie celé číslo, číslo hmotnosti. Potom odčítate počet protónov od hromadného čísla, aby ste určili počet neutrónov. - Napríklad: Atómová hmotnosť železa je 55 847, takže jej hmotnostné číslo je 56. Prvok má 26 protónov. 56 (hmotnostné číslo) mínus 26 (protónov) je 30. V jednom atóme železa je zvyčajne 30 neutrónov.
- Zmena počtu neutrónov v atóme vytvára izotopy, ktoré sú ťažšou alebo ľahšou verziou atómu.



