Autor:
Mark Sanchez
Dátum Stvorenia:
3 Január 2021
Dátum Aktualizácie:
1 V Júli 2024

Obsah
- Kroky
- Metóda 1 z 2: Stanovenie hmotnostného percenta na základe špecifikovaných hmotností
- Metóda 2 z 2: Stanovenie hmotnostného percenta, ak nie sú uvedené žiadne hmotnosti
Hmotnostné percento udáva percento prvkov v chemickej zlúčenine. Na zistenie hmotnostného percenta potrebujete poznať molárnu hmotnosť (v gramoch na mol) prvkov obsiahnutých v zlúčenine alebo počet gramov každej zložky potrebný na získanie daného roztoku.Hmotnostné percento sa vypočíta celkom jednoducho: stačí hmotnosť prvku (alebo zložky) vydeliť hmotnosťou celej zlúčeniny (alebo roztoku).
Kroky
Metóda 1 z 2: Stanovenie hmotnostného percenta na základe špecifikovaných hmotností
 1 Vyberte rovnicu na určenie hmotnostných percent chemickej zlúčeniny. Hmotnostné percento sa vypočíta podľa nasledujúceho vzorca: hmotnostné percento = (hmotnosť zložky / celková hmotnosť zlúčeniny) x 100. Na získanie percenta sa výsledok delenia vynásobí 100.
1 Vyberte rovnicu na určenie hmotnostných percent chemickej zlúčeniny. Hmotnostné percento sa vypočíta podľa nasledujúceho vzorca: hmotnostné percento = (hmotnosť zložky / celková hmotnosť zlúčeniny) x 100. Na získanie percenta sa výsledok delenia vynásobí 100. - Na začiatku riešenia problému napíšte rovnosť: hmotnostné percento = (hmotnosť zložky / celková hmotnosť zlúčeniny) x 100.
- Hmotnosť komponentu, ktorý vás zaujíma, by mala byť v stave problému. Ak nie je uvedená žiadna hmotnosť, preskočte na ďalšiu časť, ktorá vysvetľuje, ako určiť hmotnostné percento s neznámou hmotnosťou.
- Celková hmotnosť chemickej zlúčeniny sa zistí sčítaním hmotností všetkých prvkov (zložiek), ktoré sú súčasťou tejto zlúčeniny (alebo roztoku).
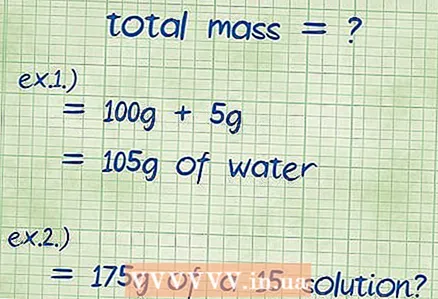 2 Vypočítajte celkovú hmotnosť zlúčeniny. Ak poznáte hmotnosti všetkých zložiek, ktoré tvoria zlúčeninu, jednoducho ich sčítajte a týmto spôsobom zistíte celkovú hmotnosť výslednej zlúčeniny alebo roztoku. Túto hmotnosť použijete ako menovateľ vo svojej rovnici pre hmotnostné percentá.
2 Vypočítajte celkovú hmotnosť zlúčeniny. Ak poznáte hmotnosti všetkých zložiek, ktoré tvoria zlúčeninu, jednoducho ich sčítajte a týmto spôsobom zistíte celkovú hmotnosť výslednej zlúčeniny alebo roztoku. Túto hmotnosť použijete ako menovateľ vo svojej rovnici pre hmotnostné percentá. - Príklad 1: Aké je hmotnostné percento 5 gramov hydroxidu sodného rozpusteného v 100 gramoch vody?
- Celková hmotnosť roztoku sa rovná súčtu množstva hydroxidu sodného a vody: 100 g + 5 g poskytne 105 g.
- Príklad 2: Koľko chloridu sodného a vody potrebujete na výrobu 175 gramov 15 -percentného roztoku?
- V tomto prípade je uvedená celková hmotnosť a požadované percento a je potrebné nájsť množstvo látky, ktoré je potrebné pridať do roztoku. Celková hmotnosť je 175 gramov.
- Príklad 1: Aké je hmotnostné percento 5 gramov hydroxidu sodného rozpusteného v 100 gramoch vody?
 3 Určte hmotnosť určeného komponentu. Ak sa od vás požaduje výpočet „hmotnostných percent“, mali by ste zistiť, koľko percent z celkovej hmotnosti látky tvorí hmotnosť určitej zložky. Zaznamenajte hmotnosť určeného komponentu. Toto bude čitateľ vo vzorci hmotnostného percenta.
3 Určte hmotnosť určeného komponentu. Ak sa od vás požaduje výpočet „hmotnostných percent“, mali by ste zistiť, koľko percent z celkovej hmotnosti látky tvorí hmotnosť určitej zložky. Zaznamenajte hmotnosť určeného komponentu. Toto bude čitateľ vo vzorci hmotnostného percenta. - Príklad 1: Hmotnosť danej zložky - hydrochloridu sodného - je 5 gramov.
- Príklad 2: V tomto prípade je hmotnosť danej zložky neznáma a musí sa nájsť.
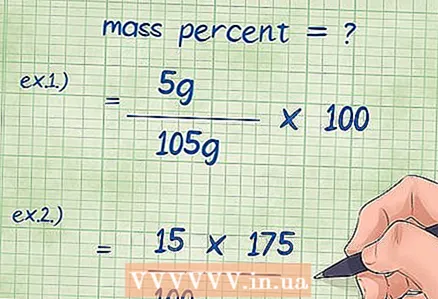 4 Zapíšte hodnoty do rovnice hmotnostných percent. Potom, čo ste určili všetky požadované hodnoty, zapojte ich do vzorca.
4 Zapíšte hodnoty do rovnice hmotnostných percent. Potom, čo ste určili všetky požadované hodnoty, zapojte ich do vzorca. - Príklad 1: hmotnostné percento = (hmotnosť zložky / celková hmotnosť zlúčeniny) x 100 = (5 g / 105 g) x 100.
- Príklad 2: Je potrebné transformovať vzorec na hmotnostné percentá tak, aby bolo možné nájsť neznámu hmotnosť chemickej zložky: hmotnosť zložky = (hmotnostné percento * celková hmotnosť zlúčeniny) / 100 = (15 * 175) / 100.
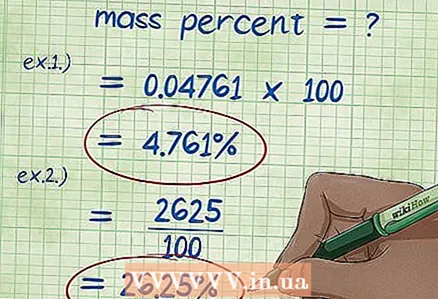 5 Vypočítajte hmotnostné percento. Po nahradení všetkých hodnôt vo vzorci hmotnostným percentom vykonajte potrebné výpočty. Hmotnosť zložky sa vydelí celkovou hmotnosťou chemickej zlúčeniny alebo roztoku a vynásobí sa 100. Výsledkom sú hmotnostné percentá tejto zložky.
5 Vypočítajte hmotnostné percento. Po nahradení všetkých hodnôt vo vzorci hmotnostným percentom vykonajte potrebné výpočty. Hmotnosť zložky sa vydelí celkovou hmotnosťou chemickej zlúčeniny alebo roztoku a vynásobí sa 100. Výsledkom sú hmotnostné percentá tejto zložky. - Príklad 1: (5/105) x 100 = 0,04761 x 100 = 4,761%. Hmotnostné percento 5 gramov hydrochloridu sodného rozpusteného v 100 gramoch vody je 4,761%.
- Príklad 2: Prepísaný výraz pre hmotnostné percento zložky je (hmotnostné percento * celková hmotnosť látky) / 100, z ktorého zistíme: (15 * 175) / 100 = (2625) / 100 = 26,25 gramov chloridu sodného.
- Potrebné množstvo vody zistíme odčítaním hmotnosti zložky od celkovej hmotnosti roztoku: 175 - 26,25 = 148,75 gramov vody.
Metóda 2 z 2: Stanovenie hmotnostného percenta, ak nie sú uvedené žiadne hmotnosti
 1 Vyberte vzorec pre hmotnostné percentá chemickej zlúčeniny. Základná rovnica na zistenie hmotnostných percent je nasledovná: hmotnostné percento = (molárna hmotnosť prvku / celková molekulová hmotnosť zlúčeniny) x 100. Molárna hmotnosť látky je hmotnosť jedného mólu danej látky, zatiaľ čo molekulová hmotnosť je hmotnosť jedného molu celého chemického spojenia. Rozdelenie sa vynásobí 100, aby sa získali percentá.
1 Vyberte vzorec pre hmotnostné percentá chemickej zlúčeniny. Základná rovnica na zistenie hmotnostných percent je nasledovná: hmotnostné percento = (molárna hmotnosť prvku / celková molekulová hmotnosť zlúčeniny) x 100. Molárna hmotnosť látky je hmotnosť jedného mólu danej látky, zatiaľ čo molekulová hmotnosť je hmotnosť jedného molu celého chemického spojenia. Rozdelenie sa vynásobí 100, aby sa získali percentá. - Na začiatku riešenia problému napíšte rovnosť: hmotnostné percento = (molárna hmotnosť prvku / celková molekulová hmotnosť zlúčeniny) x 100.
- Obe množstvá sa merajú v gramoch na mol (g / mol).
- Ak vám nie sú dané hmotnosti, hmotnostné percento prvku v danej látke sa dá zistiť pomocou molárnej hmotnosti.
- Príklad 1: Nájdite hmotnostné percento vodíka v molekule vody.
- Príklad 2: Nájdite hmotnostné percento uhlíka v molekule glukózy.
 2 Napíšte chemický vzorec. Ak v príklade nie sú uvedené chemické vzorce uvedených látok, mali by ste ich napísať sami. Ak úloha obsahuje potrebné vzorce pre chemické látky, môžete tento krok preskočiť a prejsť priamo na ďalší krok (nájsť hmotnosť každého prvku).
2 Napíšte chemický vzorec. Ak v príklade nie sú uvedené chemické vzorce uvedených látok, mali by ste ich napísať sami. Ak úloha obsahuje potrebné vzorce pre chemické látky, môžete tento krok preskočiť a prejsť priamo na ďalší krok (nájsť hmotnosť každého prvku). - Príklad 1: Napíšte chemický vzorec vody, H2O.
- Príklad 2: Napíšte chemický vzorec glukózy, C6H12O6.
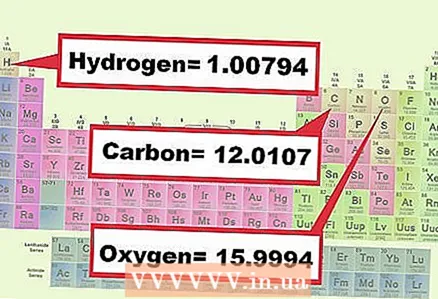 3 Nájdite hmotnosť každého prvku v zlúčenine. Určte molárnu hmotnosť každého prvku v chemickom vzorci podľa periodickej tabuľky. Hmotnosť prvku je spravidla uvedená pod jeho chemickým symbolom. Zapíšte si molárne hmotnosti všetkých prvkov, ktoré tvoria príslušnú zlúčeninu.
3 Nájdite hmotnosť každého prvku v zlúčenine. Určte molárnu hmotnosť každého prvku v chemickom vzorci podľa periodickej tabuľky. Hmotnosť prvku je spravidla uvedená pod jeho chemickým symbolom. Zapíšte si molárne hmotnosti všetkých prvkov, ktoré tvoria príslušnú zlúčeninu. - Príklad 1: Nájdite molárne hmotnosti kyslíka (15,9994) a vodíka (1,0079).
- Príklad 2: Nájdite molárne hmotnosti uhlíka (12,0107), kyslíka (15,9994) a vodíka (1,0079).
 4 Vynásobte molárnu hmotnosť každého prvku jeho molárnou frakciou. Určte, koľko mólov každého prvku je obsiahnutých v danej chemikálii, to znamená molárne zlomky prvkov. Molárne zlomky sú dané číslami v spodnej časti symbolov prvkov vo vzorci. Vynásobte molárnu hmotnosť každého prvku jeho molárnou frakciou.
4 Vynásobte molárnu hmotnosť každého prvku jeho molárnou frakciou. Určte, koľko mólov každého prvku je obsiahnutých v danej chemikálii, to znamená molárne zlomky prvkov. Molárne zlomky sú dané číslami v spodnej časti symbolov prvkov vo vzorci. Vynásobte molárnu hmotnosť každého prvku jeho molárnou frakciou. - Príklad 1: pod symbolom vodíka sú 2 a pod symbolom kyslíka je 1 (ekvivalent k absencii čísla). Molárna hmotnosť vodíka by sa teda mala vynásobiť 2: 1,00794 X 2 = 2,01588; necháme molárnu hmotnosť kyslíka rovnakú, 15,9994 (to znamená, vynásobte 1).
- Príklad 2: pod symbolom uhlíka je 6, pod vodíkom 12 a pod kyslíkom 6. Vynásobením molárnej hmotnosti prvkov týmito číslami nájdeme:
- uhlík: (12,0107 * 6) = 72,0642
- vodík: (1,00794 * 12) = 12,09528
- kyslík: (15,9994 * 6) = 95,9964
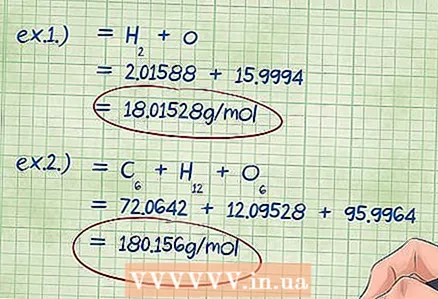 5 Vypočítajte celkovú hmotnosť zlúčeniny. Sčítajte nájdené hmotnosti všetkých prvkov zahrnutých v tejto zlúčenine. Súčet molárnych hmotností prvkov vynásobený molárnymi frakciami vám poskytne celkovú hmotnosť chemickej zlúčeniny. Toto číslo je deliteľom vo vzorci pre hmotnostné percentá.
5 Vypočítajte celkovú hmotnosť zlúčeniny. Sčítajte nájdené hmotnosti všetkých prvkov zahrnutých v tejto zlúčenine. Súčet molárnych hmotností prvkov vynásobený molárnymi frakciami vám poskytne celkovú hmotnosť chemickej zlúčeniny. Toto číslo je deliteľom vo vzorci pre hmotnostné percentá. - Príklad 1: Pridajte k 2,01588 g / mol (hmotnosť dvoch mólov atómov vodíka) 15,9994 g / mol (hmotnosť jedného mólu atómov kyslíka), výsledok je 18,01528 g / mol.
- Príklad 2: Pridajte zistené molárne hmotnosti: uhlík + vodík + kyslík = 72,0642 + 12,09528 + 95,9964 = 180,156 g / mol.
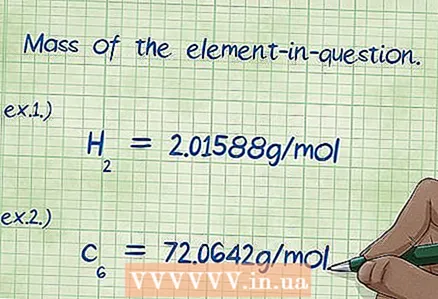 6 Určte hmotnosť prvku záujmu. Ak sa zobrazí výzva na nájdenie „hmotnostného percenta“, mali by ste vypočítať hmotnosť určitého prvku, ktorý je súčasťou zlúčeniny, ako percento z celkovej hmotnosti všetkých prvkov. Nájdite hmotnosť daného prvku a zapíšte si ho. Na to je potrebné vynásobiť molárnu hmotnosť prvku jeho molárnou frakciou. Výsledkom je, že v hmotnostnom percente získate hodnotu v čitateľovi vzorca.
6 Určte hmotnosť prvku záujmu. Ak sa zobrazí výzva na nájdenie „hmotnostného percenta“, mali by ste vypočítať hmotnosť určitého prvku, ktorý je súčasťou zlúčeniny, ako percento z celkovej hmotnosti všetkých prvkov. Nájdite hmotnosť daného prvku a zapíšte si ho. Na to je potrebné vynásobiť molárnu hmotnosť prvku jeho molárnou frakciou. Výsledkom je, že v hmotnostnom percente získate hodnotu v čitateľovi vzorca. - Príklad 1: Hmotnosť vodíka v zlúčenine je 2,01588 g / mol (hmotnosť dvoch mólov atómov vodíka).
- Príklad 2: Hmotnosť uhlíka v zlúčenine je 72,0642 g / mol (hmotnosť šiestich mólov atómov uhlíka).
 7 Nahraďte číselné hodnoty do rovnice hmotnostných percent. Potom, čo určíte hodnoty všetkých veličín, vložte ich do vzorca, ktorý bol uvedený v prvom kroku: hmotnostné percento = (molárna hmotnosť prvku / celková molekulová hmotnosť zlúčeniny) x 100.
7 Nahraďte číselné hodnoty do rovnice hmotnostných percent. Potom, čo určíte hodnoty všetkých veličín, vložte ich do vzorca, ktorý bol uvedený v prvom kroku: hmotnostné percento = (molárna hmotnosť prvku / celková molekulová hmotnosť zlúčeniny) x 100. - Príklad 1: hmotnostné percento = (molárna hmotnosť prvku / celková molekulová hmotnosť zlúčeniny) x 100 = (2,01588 / 18,01528) x 100.
- Príklad 2: hmotnostné percento = (molárna hmotnosť prvku / celková molekulová hmotnosť zlúčeniny) x 100 = (72,0642 / 180,156) x 100.
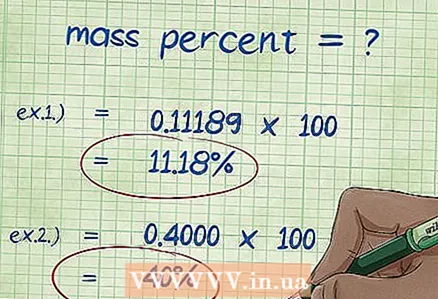 8 Vypočítajte hmotnostné percento. Po nahradení číselných hodnôt vykonajte požadované aritmetické operácie.Hmotnosť prvku vydelíme celkovou hmotnosťou zlúčeniny a vynásobíme 100. Výsledkom je hmotnostné percento prvku.
8 Vypočítajte hmotnostné percento. Po nahradení číselných hodnôt vykonajte požadované aritmetické operácie.Hmotnosť prvku vydelíme celkovou hmotnosťou zlúčeniny a vynásobíme 100. Výsledkom je hmotnostné percento prvku. - Príklad 1: hmotnostné percento = (molárna hmotnosť prvku / celková molekulová hmotnosť zlúčeniny) x 100 = (2,01588 / 18,01528) x 100 = 0,111189 x 100 = 11,18%. Hmotnostné percento atómov vodíka v molekule vody je 11,18%.
- Príklad 2: hmotnostné percento = (molárna hmotnosť prvku / celková molekulová hmotnosť zlúčeniny) x 100 = (72,0642 / 180,156) x 100 = 0,4000 x 100 = 40,00%. Hmotnostné percento atómov uhlíka v molekule glukózy je 40,00%.