Obsah
- Na krok
- Metóda 1 z 3: Začnite
- Metóda 2 z 3: Ako určíte hmotnostné percento pre dané hmotnosti
- Metóda 3 z 3: Ako zistíte hmotnostné percento, ak nie sú uvedené hmotnosti
- Tipy
Budete požiadaní, aby ste určili „hmotnostné percento“ konkrétnej chemikálie pre chemický test. Pred panikou najskôr čítajte. Je to oveľa jednoduchšie, ako to znie.
Na krok
Metóda 1 z 3: Začnite
Hmotnostné percento je hmotnosť konkrétnej chemikálie vydelená celkovou hmotnosťou všetkých chemikálií v roztoku / zlúčenine vyjadrená v percentách. Existujú dva spôsoby, ako pristupovať k tejto hromadnej percentuálnej otázke. Ďalej sa dozviete, aký prístup zvoliť.
- Zistite, či vám otázka, ktorú musíte vyriešiť, dáva množstvo chemikálií alebo nie.
- Keď sú dané omše. Ak je v otázke už uvedené množstvo chemických látok, tak ako v „Aké je hmotnostné percento 5 g hydroxidu sodného rozpusteného v 100 g vody?“potom postupujte podľa pokynov popísaných nižšie v časti „Ako určiť hmotnostné percento pre dané hmotnosti“.
- Ak nie sú uvedené hmotnosti. Niekedy budete požiadaní, aby ste poskytli hmotnostné percento, ale hmotnosť chemikálií nie je známa. V týchto prípadoch použijete chemické vzorce na rozpustenie chemických hmôt. Takáto otázka môže vyzerať takto, „Určiť hmotnostné percento vodíka v molekule vody?“ Ak je to tak, postupujte podľa pokynov v časti „Ako určiť hmotnostné percento, ak nie sú uvedené hmotnosti“.
Metóda 2 z 3: Ako určíte hmotnostné percento pre dané hmotnosti
Ďalej nájdete kroky potrebné na vyriešenie otázky týkajúcej sa percentuálneho podielu hmoty, kde je uvedená hmotnosť chemických látok. Takáto otázka môže vyzerať takto, „Aké je hmotnostné percento 5 g hydroxidu sodného rozpusteného v 100 g vody?“ Príklady v tejto časti sú venované tejto otázke.
 Vypočítajte celkovú hmotnosť. Sčítajte všetky hmotnosti všetkých prvkov v zlúčenine alebo roztoku. Takto získate celkovú hmotnosť. Toto je menovateľ. Zapíšte si ich.
Vypočítajte celkovú hmotnosť. Sčítajte všetky hmotnosti všetkých prvkov v zlúčenine alebo roztoku. Takto získate celkovú hmotnosť. Toto je menovateľ. Zapíšte si ich. - Napríklad v tomto kroku urobíte 100 g + 5 g pre celkovú hmotnosť 105 g.
 Určte, čo je požadovaná chemikália. Keď sa zobrazí výzva na vyhľadanie „percenta hmotnosti“, zobrazí sa výzva na určenie hmotnosti konkrétnej chemikálie (požadovanej chemikálie) ako percentuálneho podielu z celkovej hmotnosti všetkých prvkov. Zistite, o akú chemickú látku ide. Zapíšte si ich. Toto je váš pult.
Určte, čo je požadovaná chemikália. Keď sa zobrazí výzva na vyhľadanie „percenta hmotnosti“, zobrazí sa výzva na určenie hmotnosti konkrétnej chemikálie (požadovanej chemikálie) ako percentuálneho podielu z celkovej hmotnosti všetkých prvkov. Zistite, o akú chemickú látku ide. Zapíšte si ich. Toto je váš pult. - Napríklad v tomto kroku zistíte, že požadovaná chemikália je 5 g hydroxidu sodného.
 Zdieľam. Hmotnosť požadovanej chemikálie, ktorá sa nachádza v kroku „Určenie požadovanej chemikálie“, vydelte celkovou hmotnosťou vypočítanou v časti „Vypočítajte celkovú hmotnosť“. Výsledkom tohto rozdelenia je omša.
Zdieľam. Hmotnosť požadovanej chemikálie, ktorá sa nachádza v kroku „Určenie požadovanej chemikálie“, vydelte celkovou hmotnosťou vypočítanou v časti „Vypočítajte celkovú hmotnosť“. Výsledkom tohto rozdelenia je omša. - Napríklad v tomto kroku vydelíte 5 g (hmotnosť hydroxidu sodného) číslom 105 (celková hmotnosť), aby ste dostali hmotnostný pomer, 0,04761.
 Vypočítajte percento. Vynásobte pomer zistenej hmotnosti číslom 100. Takto získate hmotnostné percento.
Vypočítajte percento. Vynásobte pomer zistenej hmotnosti číslom 100. Takto získate hmotnostné percento. - Napríklad v tomto kroku vynásobíte 0,04761 číslom 100 a získate 4,761%. Hmotnostné percento 5 gramov hydroxidu sodného rozpusteného v 100 gramoch vody je teda 4,761%.
Metóda 3 z 3: Ako zistíte hmotnostné percento, ak nie sú uvedené hmotnosti
Ďalej nájdete kroky potrebné na vyriešenie otázky týkajúce sa hmotnostných percent, kde nie sú uvedené chemické hmotnosti. Takáto otázka môže vyzerať takto, „Určiť hmotnostné percento vodíka v molekule vody?Príklady v tejto časti rozpracovávajú tento problém.
 Prečítajte si nasledujúce definície. Predtým, ako budete môcť vypočítať hmotnostné percento v takomto výkaze, musíte porozumieť chemickým konceptom uvedeným nižšie.
Prečítajte si nasledujúce definície. Predtým, ako budete môcť vypočítať hmotnostné percento v takomto výkaze, musíte porozumieť chemickým konceptom uvedeným nižšie. - Kompozitné tkaniny. Zlúčenina vzniká spojením dvoch alebo viacerých rôznych chemických prvkov. Tieto prvky sú držané spolu kovalentnými väzbami alebo iónovými väzbami. Prvky v kompozitných materiáloch je možné opäť separovať chemickou reakciou.
- Napríklad Vodík a kyslík sú rôzne chemické prvky. Molekula vody je preto zložená látka, pretože pozostáva z dvoch atómov vodíka a jedného atómu kyslíka.
- Chemické vzorce. Zlúčenina môže byť uvedená v skrátenej forme. Toto sa nazýva chemický vzorec. Chemický vzorec zohľadňuje aj relatívne množstvo každého atómu v zlúčenine.
- Napríklad Chemický vzorec vody pozostáva z „H“ pre vodík a „O“ pre kyslík. Pretože na každom atóme kyslíka v molekule vody sú dva atómy vodíka, chemický vzorec vody by mal pozostávať z dvoch H na O. Chemický vzorec vody sa teda píše ako H2O.
- Molárny pomer. Relatívne množstvo jedného typu atómu v porovnaní s iným typom atómu v zlúčenine sa nazýva počet mólov. Nájdete to pri pohľade na chemický vzorec zlúčeniny.
- Napríklad Chemický vzorec vody je H2O. Rozkladom tohto vzorca vieme, že molárny pomer vodíka a kyslíka v molekule vody sa rovná 2: 1.
- Kompozitné tkaniny. Zlúčenina vzniká spojením dvoch alebo viacerých rôznych chemických prvkov. Tieto prvky sú držané spolu kovalentnými väzbami alebo iónovými väzbami. Prvky v kompozitných materiáloch je možné opäť separovať chemickou reakciou.
 Napíšte chemický vzorec. Možno boli dané chemické vzorce, ale ak to tak nie je, najskôr si zapíšte chemické vzorce každej požadovanej zlúčeniny. Ak sú uvedené chemické vzorce, môžete tento krok preskočiť a pokračovať krokom „Určenie hmotnosti každého prvku“.
Napíšte chemický vzorec. Možno boli dané chemické vzorce, ale ak to tak nie je, najskôr si zapíšte chemické vzorce každej požadovanej zlúčeniny. Ak sú uvedené chemické vzorce, môžete tento krok preskočiť a pokračovať krokom „Určenie hmotnosti každého prvku“. - Napríklad v tomto kroku musíte napísať chemický vzorec vody ako H2O.
 Určuje hmotnosť každého prvku. Vyhľadajte molekulovú hmotnosť každého prvku v chemickom vzorci v periodickej tabuľke. Zapíšte si ich.
Určuje hmotnosť každého prvku. Vyhľadajte molekulovú hmotnosť každého prvku v chemickom vzorci v periodickej tabuľke. Zapíšte si ich. - Napríklad v tomto kroku hľadáte molekulovú hmotnosť kyslíka 15,9994; a molekulová hmotnosť vodíka 1,00794.
 Vynásobte hmotnosti molárnym pomerom. Určte, koľko mólov je v každom prvku zlúčeniny. Vynásobte molárnu hmotnosť molárnym pomerom. Zapíšte si ich.
Vynásobte hmotnosti molárnym pomerom. Určte, koľko mólov je v každom prvku zlúčeniny. Vynásobte molárnu hmotnosť molárnym pomerom. Zapíšte si ich. - Napríklad v tomto kroku je molárny pomer vodíka a kyslíka vo vode 2: 1.Preto vynásobíte molárnu hmotnosť vodíka 2,100794 X 2 = 2,01588; a ponechať molárnu hmotnosť kyslíka tak, ako je, 15,9994.
 Vypočítajte celkovú hmotnosť. Pridajte celkovú hmotnosť všetkých prvkov vo vašej zmesi. Na zaistenie správnych molárnych pomerov nezabudnite použiť hmotnosti z kroku „Vynásobte hmotnosti molárnym pomerom“. Zapíšte si ich. Toto bude váš menovateľ.
Vypočítajte celkovú hmotnosť. Pridajte celkovú hmotnosť všetkých prvkov vo vašej zmesi. Na zaistenie správnych molárnych pomerov nezabudnite použiť hmotnosti z kroku „Vynásobte hmotnosti molárnym pomerom“. Zapíšte si ich. Toto bude váš menovateľ. - Napríklad v tomto kroku pridáte 2,01588 (hmotnosť 2 mólov atómov vodíka) o 15,9994 (hmotnosť 1 mólu atómov kyslíka) a získate 18,01528.
 Stanovte požadovanú chemikáliu. Keď sa zobrazí výzva na výpočet „hmotnostného percenta“, zobrazí sa výzva na určenie hmotnosti konkrétnej chemikálie (požadovanej chemikálie) ako percentuálneho podielu z celkovej hmotnosti všetkých prvkov. Stanovte požadovanú chemikáliu. Zapíšte si ich. Toto je menovateľ.
Stanovte požadovanú chemikáliu. Keď sa zobrazí výzva na výpočet „hmotnostného percenta“, zobrazí sa výzva na určenie hmotnosti konkrétnej chemikálie (požadovanej chemikálie) ako percentuálneho podielu z celkovej hmotnosti všetkých prvkov. Stanovte požadovanú chemikáliu. Zapíšte si ich. Toto je menovateľ. - Napríklad v tomto kroku zistíte, že požadovanou chemikáliou je vodík.
 Zdieľam. Vydeľte hmotnosť požadovanej chemikálie z kroku „Určenie požadovanej chemikálie“ celkovou hmotnosťou vypočítanou v časti „Vypočítajte celkovú hmotnosť“. Toto vypočítané číslo je hmotnostný pomer.
Zdieľam. Vydeľte hmotnosť požadovanej chemikálie z kroku „Určenie požadovanej chemikálie“ celkovou hmotnosťou vypočítanou v časti „Vypočítajte celkovú hmotnosť“. Toto vypočítané číslo je hmotnostný pomer. - Napríklad v tomto kroku vydelíte 2,01588 (hmotnosť atómov vodíka) 18,01528 (celková hmotnosť molekuly vody). Takto získate hmotnostný pomer 0,111189.
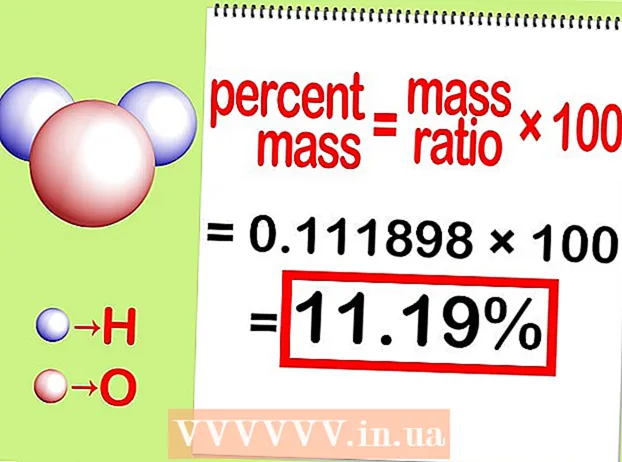
 Vypočítajte percento. Vynásobte výsledný pomer hmotnosti z kroku „Rozdeliť“ o 100. Získate tak odpoveď, hmotnostné percento.
Vypočítajte percento. Vynásobte výsledný pomer hmotnosti z kroku „Rozdeliť“ o 100. Získate tak odpoveď, hmotnostné percento. - Napríklad v tomto kroku vynásobíte 0,111189 číslom 100 a získate 11,18%. Hmotnostné percento atómov vodíka v molekule vody je 11,18%.
Tipy
- V kroku „Napíšte chemický vzorec“ sa uistite, či je váš chemický vzorec vyvážený. Ak je uvedený chemický vzorec, mal by byť v rovnováhe. Ak vás však najskôr požiadali o vyriešenie chemickej rovnice, aby ste vytvorili uvedený chemický vzorec, pred určením hmotnostného percenta sa uistite, že je vyvážená.