Autor:
Monica Porter
Dátum Stvorenia:
22 Pochod 2021
Dátum Aktualizácie:
1 V Júli 2024

Obsah
Hmotnostné percento označuje percento každého prvku v chemickej zlúčenine. Ak chcete zistiť hmotnostné percento, musíte poznať molárnu hmotnosť prvkov v zlúčenine v gramoch / mol alebo počet gramov látok, z ktorých sa roztok skladá. Hmotnostné percento sa počíta pomocou jednoduchého vzorca, ktorým je vydelenie hmotnosti prvku (alebo rozpustenej látky) hmotnosťou zlúčeniny (alebo roztoku).
Kroky
Metóda 1 z 2: Vypočítajte hmotnostné percento so známou hmotnosťou
Stanovte rovnicu pre percento hmotnosti v zmesi. Základný vzorec pre výpočet hmotnostného percenta v zmesi je: hmotnostné percento = (kvalitná hmotnosť / zmiešaná hmotnosť) x 100. Nakoniec musíte percentuálny podiel vynásobiť číslom 100.
- Keď začnete riešiť problém, napíšte rovnicu: hmotnostné percento = (hmotnosť látky / zmiešaná hmotnosť) x 100.
- Množstvo kvality bude uvedené v probléme. Ak téma nie je zadaná, v nasledujúcej časti nájdete informácie o tom, ako nájsť hmotnostné percentá bez znalosti váh.
- Hmotnosť zmesi sa rovná celkovej hmotnosti látok, ktoré tvoria zmes alebo roztok.

Vypočítajte hmotnosť zmesi. Keď poznáte množstvo prvkov alebo zlúčenín, musíte ich iba spočítať a získať tak hmotnosť výslednej zmesi alebo roztoku. Toto je menovateľ vo vzorci percenta hmotnosti.- Príklad 1: Aké je hmotnostné percento 5 g hydroxidu sodného po rozpustení v 100 g vody?
- Hmotnosť zmesi je celková hmotnosť hydroxidu sodného a vody: 100 g + 5 g. Zmiešaná hmotnosť je teda 105 g.
- Príklad 2: Aké množstvo chloridu sodného a vody je potrebné na vytvorenie 175 g 15% roztoku?
- V tomto príklade, kde poznáte zmiešanú hmotnosť a hmotnostné percento, sa vás úloha spýta na nájdenie hmotnosti pridanej rozpustenej látky. Hmotnosť zmesi je 175 g.
- Príklad 1: Aké je hmotnostné percento 5 g hydroxidu sodného po rozpustení v 100 g vody?

Určte hmotnosť látky, aby ste zistili percentuálnu hmotnosť. Keď kvíz žiada o nájdenie „hmotnostného percenta“ látky, musíte nájsť hmotnosť látky ako percento z celkovej hmotnosti všetkých zložiek. Zapíšte si hmotnosť látky a zistite percentuálnu hmotnosť. Toto je čitateľ vo vzorci pre percentuálnu hmotnosť.- Príklad 1: Hmotnosť hydroxidu sodného (látka zistená hmotnostným zlomkom) je 5 g.
- Príklad 2: V tomto príklade množstvo látky hľadá percento neznámej hmotnosti a vy ju hľadáte.

Nahraďte premenné rovnicou hmotnostných percent. Len čo určíte hodnotu každej premennej, jednoducho ich zapojte do rovnice.- Príklad 1: hmotnostné percento = (hmotnosť látky / zmiešaná hmotnosť) x 100 = (5 g / 105 g) x 100.
- Príklad 2: Potrebujeme previesť rovnicu percenta hmotnosti na výpočet množstva neznámej kvality: kvalita hmotnosť = (percentuálna hmotnosť * zmiešaná hmotnosť) / 100 = (15 * 175) / 100 .
Vypočítajte objemové percento. Teraz, keď je rovnica naplnená, musíte vypočítať iba hmotnostné percento. Hmotnosť látky sa vydelí hmotou zmesi a potom sa vynásobí číslom 100. Toto je hmotnostné percento látky v zmesi.
- Príklad 1: (5/105) x 100 = 0,04761 x 100 = 4,761%. Hmotnostné percento 5 g hydroxidu sodného rozpusteného v 100 g vody je teda 4 761%.
- Príklad 2: Rovnica po prepočte na výpočet množstva kvality je (percentuálna hmotnosť * zmiešaná hmotnosť) / 100: (15 * 175) / 100 = (2625) / 100 = 26,25 gramov chlorid sodný.
- Hmotnosť pridanej vody je hmotnosť zmesi mínus hmotnosť látky: 175 - 26,25 = 148,75 gramov vody.
Metóda 2 z 2: Výpočet hmotnostného percenta, ak hmotnosť nie je známa
Stanovte rovnicu pre percento hmotnosti v zlúčenine. Základný vzorec pre výpočet hmotnostného percenta v zlúčenine je: hmotnostné percento = (elementárna molárna hmotnosť / molárna hmotnosť zlúčeniny) x 100. Elementárna molárna hmotnosť je hmotnosť jedného molu prvku zatiaľ čo molekulová hmotnosť je hmotnosť jedného molu zlúčeniny. Nakoniec musíte vynásobiť číslom 100, aby ste dostali percentuálnu hodnotu.
- Keď začnete riešiť problém, napíšte rovnicu: hmotnostné percento = (elementárna molárna hmotnosť / molárna hmotnosť zlúčeniny) x 100.
- Jednotkami vyššie uvedených dvoch hodnôt sú gramy na mol (g / mol).
- Ak problém neposkytne hmotnosť, môžete pomocou molárnej hmotnosti vypočítať hmotnostné percento prvku.
- Príklad 1: Vypočítajte hmotnostné percento vodíka v molekule vody.
- Príklad 2: Vypočítajte hmotnostné percento uhlíka v molekule glukózy.
Napíš Chemický vzorec. Ak problém nezahŕňa chemické vzorce pre každú zlúčeninu, budete si ich musieť zapísať. Ak je problém s chemickým vzorcom, tento krok preskočte a prejdite na krok „Vyhľadajte hmotnosť každého prvku“.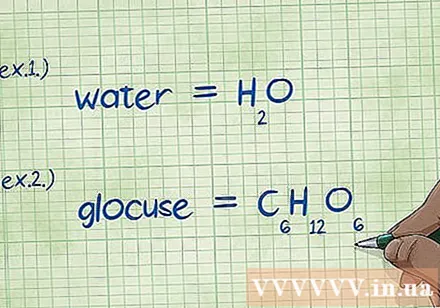
- Príklad 1: Napíšte chemický vzorec pre vodu, H2O.
- Príklad 2: Napíšte chemický vzorec pre glukózu, C6H12O6.
Nájdite hmotnosť každého prvku v zmesi. Vyhľadajte molekulovú hmotnosť každého prvku v chemickom vzorci v periodickej tabuľke. Elementárna hmotnosť je zvyčajne napísaná pod chemickým symbolom. Zapíšte hmotnosť každého prvku v zlúčenine.
- Príklad 1: Môžeme zistiť, že hmotnostný atóm kyslíka je 15 9994; a kubický atóm vodíka je 1 0079.
- Príklad 2: Zistili sme, že hmotnostný atóm uhlíka je 12 0107; kyslík je 15,9994; a vodík je 1,0079.
Vynásobte kubický atóm molárnym pomerom. Určte počet mólov (molárny pomer) každého prvku v chemickej zlúčenine. Molárny pomer sa počíta ako malý počet uvedený nižšie v chemickom vzorci zlúčeniny. Vynásobte kubický atóm každého prvku molárnym pomerom.
- Príklad 1: Vodík má dolný index dvoch, zatiaľ čo kyslík má dolný index 1. Takže vynásobte molekulovú hmotnosť vodíka číslom 2, 1 00794 X 2 = 2 01588; a molekulová hmotnosť kyslíka je 15 999 (vynásobená jednou).
- Príklad 2: Uhlík má dolný index 6, vodík 12 a kyslík 6. Vynásobte kubický atóm každého prvku indexom uvedeným nižšie.
- Uhlík (12 0107 * 6) = 72 0 642
- Vodík (1 00794 * 12) = 12 09528
- Kyslík (15 999 * 6) = 95 9964
Vypočítajte celkovú hmotnosť zlúčeniny. Pridajte hmotnosti všetkých prvkov v zlúčenine. Celkovú hmotnosť zlúčenín môžete vypočítať pomocou hmotností vyjadrených v molárnych pomeroch. Toto číslo bude menovateľom v rovnici percenta hmotnosti.
- Príklad 1: Pridajte 2 01588 g / mol (hmotnosť dvoch mólov atómov vodíka) k 15 9994 g / mol (hmotnosť jedného mólu atómov kyslíka), čo poskytne 18 01528 g / mol.
- Príklad 2: Sčítajte všetky hmotnosti dohromady: uhlík + vodík + kyslík = 72 0642 + 12 09528 + 95 9964 = 180 156 g / mol.
Určte elementárnu hmotnosť, na ktorú sa má vypočítať hmotnostné percento. Ak problém vyžaduje „hmotnostné percento“, znamená to, že musíte nájsť hmotnosť konkrétneho prvku v zlúčenine ako percento z celkovej hmotnosti všetkých prvkov. Určte a zapíšte hmotnosť prvku. Táto hmotnosť je hmotnosť vyjadrená v molárnom pomere. Toto číslo je čitateľom rovnice percenta hmotnosti.
- Príklad 1: Hmotnosť vodíka v zlúčenine je 2 01588 g / mol (hmotnosť dvoch mólov atómov vodíka).
- Príklad 2: Hmotnosť uhlíka v zlúčenine je 72 0 642 g / mol (hmotnosť šiestich mólov atómov uhlíka).
Nahraďte premenné rovnicou hmotnostných percent. Po určení hodnôt každej premennej ich jednoducho nahraďte rovnicou identifikovanou v prvom kroku: hmotnostné percento = (elementárna molárna hmotnosť / molárna hmotnosť zlúčeniny) x 100 .
- Príklad 1: hmotnostné percento = (elementárna molárna hmotnosť / molárna hmotnosť zlúčeniny) x 100 = (2,1588 / 18,1528) x 100.
- Príklad 2: hmotnostné percento = (elementárna molárna hmotnosť / molárna hmotnosť zlúčeniny) x 100 = (72 0642/180 156) x 100.
Vypočítajte objemové percento. Teraz, keď je rovnica naplnená, musíte vypočítať iba hmotnostné percento. Hmotnosť prvku sa vydelí celkovou hmotou zlúčeniny a potom sa vynásobí číslom 100. Toto je percento hmotnosti prvku v zlúčenine.
- Príklad 1: hmotnostné percento = (2 01588/18 01528) x 100 = 0,1111189 x 100 = 11,18%. Preto je hmotnostné percento atómu vodíka v molekule vody 11,18%.
- Príklad 2: hmotnostné percento = (elementárna molárna hmotnosť / molárna hmotnosť zlúčeniny) x 100 = (72 0642/180 156) x 100 = 0,4000 x 100 = 40,00%. Takže hmotnostné percento atómu uhlíka v molekule glukózy je 40,00%.