Autor:
Lewis Jackson
Dátum Stvorenia:
12 Smieť 2021
Dátum Aktualizácie:
1 V Júli 2024

Obsah
Stanovenie počtu neutrónov v atóme je dosť jednoduché, nemusíte robiť ani žiadne experimenty. Ak chcete vypočítať počet neutrónov v normálnom atóme alebo izotope, musíte mať pripravenú periodickú tabuľku a postupovať podľa pokynov.
Kroky
Metóda 1 z 2: Nájdite počet neutrónov v normálnom atóme
Určte polohu prvku na periodickej tabuľke. Ako príklad nájdeme prvok osmium (Os) v šiestom rade zhora.
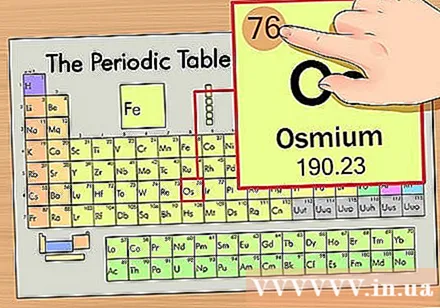
Nájdite atómové číslo prvku. Toto je najnápadnejšie číslo, ktoré platí pre každý prvok a je nad prvočíslom symbolu (na doske, ktorú používame, nie sú žiadne ďalšie čísla). Atómové číslo je počet protónov v jednom atóme tohto prvku. Os je číslo 76, čo znamená, že v atóme osmia je 76 protónov.- Počet protónov sa v prvku nikdy nemení; je to v podstate určujúca charakteristika prvku.
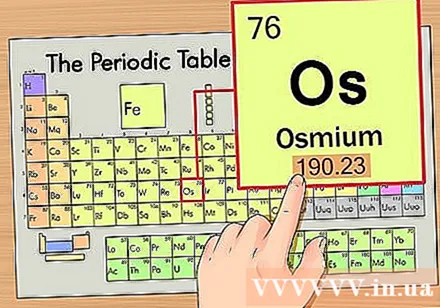
Nájdite atómovú hmotnosť prvku. Toto číslo sa zvyčajne nachádza pod prvočíslom. Upozorňujeme, že periodická tabuľka v tomto príklade má iba atómové číslo a žiadnu atómovú hmotnosť. Nie všetky periodické tabuľky. Osmium má atómovú hmotnosť 190,23.
Atómovú hmotnosť zaokrúhlite na najbližšie celé číslo a získate atómovú hmotnosť. Napríklad 190,23 by bolo zaokrúhlené na 190, takže atómová hmotnosť osmia je 190.- Atómová hmotnosť je priemerom izotopov toho istého chemického prvku, a preto zvyčajne nejde o celé číslo.
Odčítajte atómové číslo od atómovej hmotnosti. Pretože väčšina atómovej hmotnosti je hmotnosť protónov a neutrónov, odčítaním počtu protónov od atómovej hmotnosti (t. J. Atómové číslo) budete počítať získajte počet neutrónov v atóme. Číslo za desatinnou čiarkou predstavuje veľmi malé hmotnosti elektrónov v atóme. V tomto príklade máme: 190 (hmotnostný atóm) - 76 (počet protónov) = 114 (počet neutrónov).
Zapamätajte si recept. Na zistenie počtu neutrónov jednoducho použijeme nasledujúci vzorec: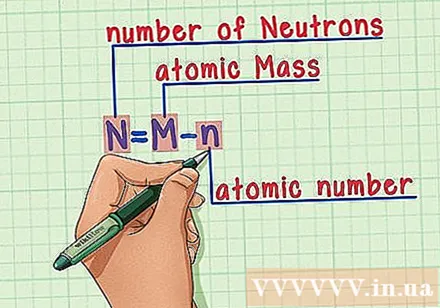
- N = M - n
- N = počet neutrónov
- M = atómová hmotnosť
- n = atómové číslo
- N = M - n
Metóda 2 z 2: Nájdite počet neutrónov v izotope
Určte polohu prvku na periodickej tabuľke. Zoberme si ako príklad prvok izotop uhlíka-14. Pretože izotopová forma uhlíka-14 je jednoducho uhlík (C), hľadajte uhlík v periodickej tabuľke (druhý rad zhora).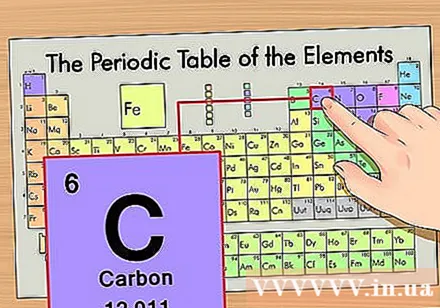
Nájdite atómové číslo prvku. Toto je najnápadnejšie číslo, ktoré platí pre každý prvok a je nad prvočíslom symbolu (na doske, ktorú používame, nie sú žiadne ďalšie čísla). Atómové číslo je počet protónov v jednom atóme tohto prvku. C je číslo 6, čo znamená, že v atóme uhlíka je 6 protónov.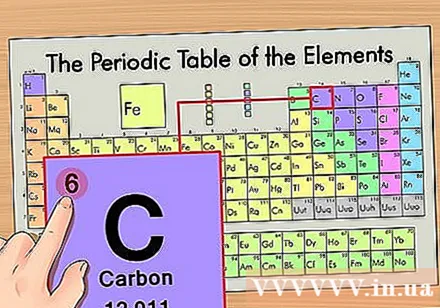
Nájdite atómovú hmotnosť. S izotopmi je to mimoriadne ľahké, pretože sú pomenované podľa atómovej hmotnosti. Napríklad uhlík-14 by mal atómovú hmotnosť 14. Keď nájdete atómovú hmotnosť izotopu, zostávajúce kroky na nájdenie počtu neutrónov budú rovnaké ako v prípade normálneho atómu.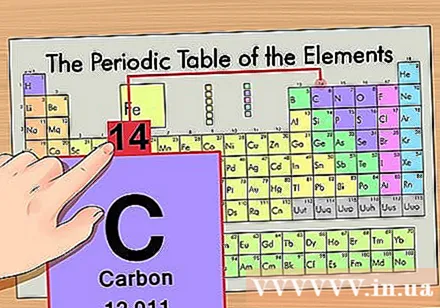
Odčítajte atómové číslo od atómovej hmotnosti. Pretože väčšina atómovej hmotnosti je hmotnosť protónov a neutrónov, odčítaním počtu protónov od atómovej hmotnosti (t. J. Atómové číslo) budete počítať získajte počet neutrónov v atóme. Číslo za desatinnou čiarkou predstavuje veľmi malé hmotnosti elektrónov v atóme. V tomto príklade máme: 14 (hmotnostný atóm) - 6 (počet protónov) = 8 (počet neutrónov).
Zapamätajte si recept. Na zistenie počtu neutrónov použijeme nasledujúci vzorec: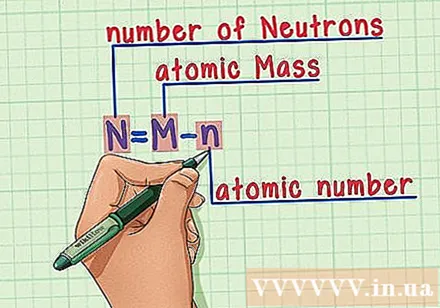
- N = M - n
- N = počet neutrónov
- M = atómová hmotnosť
- n = atómové číslo
- N = M - n
Rada
- Hmotnosť prvku je do značnej miery hmotnosť protónov a neutrónov, zatiaľ čo hmotnosť elektrónov a ďalších prvkov je zanedbateľná (takmer nulová). Pretože hmotnosť protónu je približne rovnaká ako hmotnosť neutrónu a atómové číslo predstavuje počet protónov, stačí od celkovej hmotnosti odčítať počet protónov.
- Ak si nepamätáte význam čísel v periodickej tabuľke, nezabudnite, že periodická tabuľka je zvyčajne založená na atómových číslach (t. J. Na počte protónov), začínajúcich od 1 (vodík) a zvyšujúcich jedno slovo. zľava doprava, končiace číslom 118 (ununoctium). Pretože počet protónov je poznávacím znakom každého atómu, je to najjednoduchšia vlastnosť, na ktorej sú prvky usporiadané. (Napríklad atóm s 2 protónmi je vždy hélium, rovnako ako atóm so 79 protónmi je vždy zlato.)
Zdroje a citácie
- Interaktívna periodická tabuľka



