Autor:
Randy Alexander
Dátum Stvorenia:
2 Apríl 2021
Dátum Aktualizácie:
1 V Júli 2024

Obsah
Chemická rovnica je symbolické znázornenie chemickej reakcie. Činidlá sú napísané na ľavej strane a produkt na pravej strane. Zákon zachovania hmotnosti naznačuje, že pri chemickej reakcii sa nenarodili ani nestratili žiadne atómy, takže počet atómov prítomných v reaktante musí byť rovný počtu atómov prítomných v reakcii. výrobok. Podľa tohto tutoriálu môžete vyvážiť chemické rovnice rôznymi spôsobmi.
Kroky
Metóda 1 z 2: Zostatok podľa tradičnej metódy
Napíš danú rovnicu. V tomto príklade by ste mali: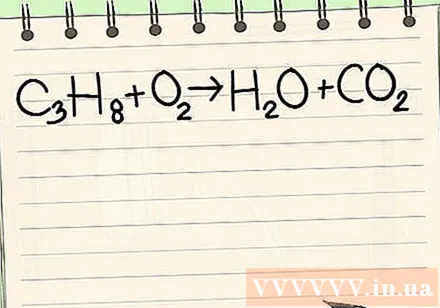
- C.3H8 + O.2 -> H2O + CO2
- Táto reakcia nastáva, keď sa propán (C3H8spaľoval v kyslíku za vzniku vody a oxidu uhličitého.

Zapíšte si počet atómov pre každý prvok, ktorý máte na každej strane rovnice. Počet atómov v rovnici nájdete podľa indexov nižšie vedľa jednotlivých atómov.- Vľavo: 3 uhlíky, 8 vodíka a 2 kyslík.
- Vpravo: 1 uhlík, 2 vodík a 3 kyslík.
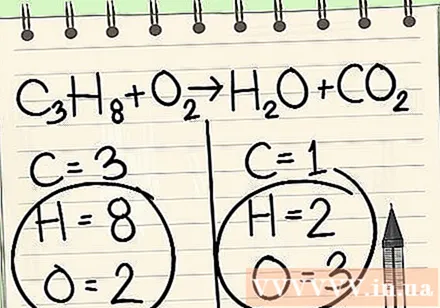
Nakoniec vždy nechajte vodík a kyslík.
Ak vám zostáva na vyrovnanie viac ako jeden prvok: Vyberte prvok, ktorý sa objaví iba v jednej molekule reaktantu a iba v jednej molekule produktu. To znamená, že najskôr budete musieť vyvážiť atómy uhlíka.
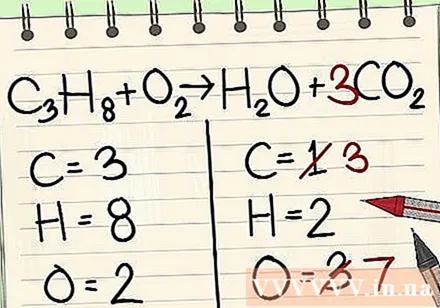
Pridajte koeficient pre jednotlivé atómy uhlíka na pravú stranu rovnice, aby ste ju vyrovnali s tromi atómami uhlíka na ľavej strane rovnice.- C.3H8 + O.2 -> H2O + 3CO2
- Faktor 3 pred uhlíkom na pravej strane naznačuje, že sú 3 atómy uhlíka, rovnako ako index pod 3 na ľavej strane označuje 3 atómy uhlíka.
- V chemickej rovnici môžete zmeniť koeficient, nie však dolný index.
Ďalej je to atómová rovnováha vodíka. Naľavo máte 8 atómov vodíka. Preto budete potrebovať 8 na pravej strane.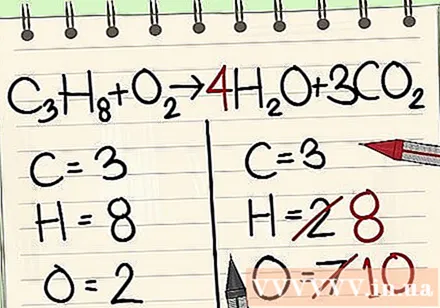
- C.3H8 + O.2 -> 4H2O + 3CO2
- Napravo od hodiny pridáte ako faktor 4, pretože spodné číslo ukazuje, že už máte 2 atómy vodíka.
- Keď vynásobíte faktor 4 indexom 2, získate 8.
- Ostatných 6 atómov kyslíka je z 3CO2(3x2 = 6 atómov kyslíka + 4 ďalšie atómy kyslíka = 10)
Rovnováha atómov kyslíka.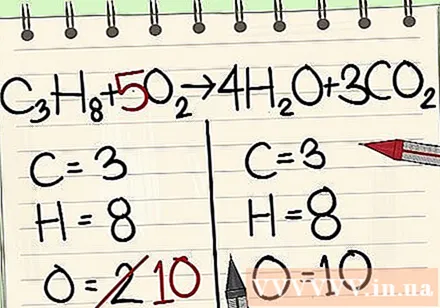
- Pretože ste do molekúl napravo od rovnice pridali koeficienty, zmenil sa počet atómov kyslíka. Teraz máte 4 molekuly kyslíka v molekule vody a 6 atómov kyslíka v molekule oxidu uhličitého. Celkovo máme 10 atómov kyslíka.
- Pridajte faktor 5 k molekule kyslíka vľavo od rovnice. Teraz máte na každej strane 10 molekúl kyslíka.
- C.3H8 + 5O2 -> 4H2O + 3CO2.

- Atómy uhlíka, vodíka a kyslíka sú v rovnováhe. Vaša rovnica je úplná.
Metóda 2 z 2: Rovnováha podľa algebraickej metódy
Píšte rovnice podľa symbolov a vzorcov. Príklad a = 1 a napíš rovnicu podľa tohto vzorca.
Nahraďte číslice ich premennými.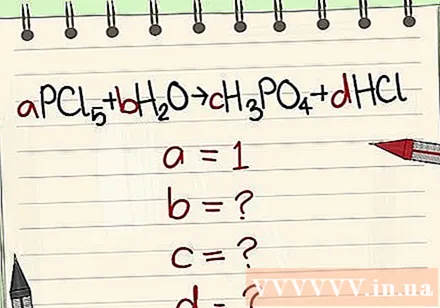
Skontrolujte množstvo prvkov na strane reakcie, ako aj na strane produktu.
- Príklad: aPCl5 + bH2O = cH3PO4 + dHCl tak, že a = 1 b = c = d = a oddelením prvkov P, Cl, H, O, takže získate a = 1 b = 4 c = 1 d = 5 .
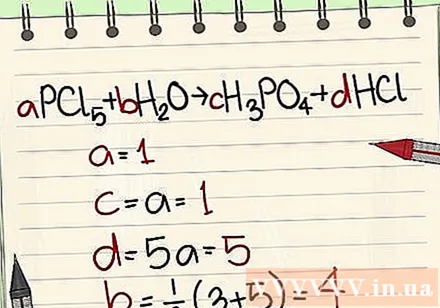
- Príklad: aPCl5 + bH2O = cH3PO4 + dHCl tak, že a = 1 b = c = d = a oddelením prvkov P, Cl, H, O, takže získate a = 1 b = 4 c = 1 d = 5 .
Rada
- Nezabudnite rovnicu zjednodušiť.
- Ak máte ťažkosti, môžete do nástroja na online vyváženie zadať rovnicu a vyvážiť ju. Pamätajte, že keď sa chystáte na skúšku, nemáte prístup k online zostatku, takže na to nezáleží.
Výstraha
- Nikdy nepoužívajte koeficient ako zlomok v chemickej rovnici - nemôžete rozdeliť molekuly alebo atómy v chemickej reakcii.
- Počas procesu rovnováhy môžete použiť zlomky, ale rovnica nebude vyvážená, ak sú koeficienty stále zlomkami.
- Ak chcete odstrániť zlomky, vynásobte celú rovnicu (ľavú aj pravú) menovateľom zlomku.